Notice
Nom du médicament vétérinaire
Vetmedin®
1,5 mg/ml solution buvable pour chiens
Composition
Chaque ml contient :
Substance active :
Pimobendane : 1,5 mg
Excipients :
Acide sorbique (E200) : 3,0 mg
Acide ascorbique (E300) : 7,0 mg
Solution limpide, incolore à jaune à légèrement vert, à légèrement brun.
Espèces cibles
Chiens.
Indications d’utilisation
Traitement de l’insuffisance cardiaque congestive canine due à une cardiomyopathie dilatée (CMD) ou à une insuffisance valvulaire (régurgitation valvulaire mitrale et/ou tricuspide).
Traitement de la cardiomyopathie dilatée au stade préclinique (asymptomatique avec augmentation du diamètre ventriculaire gauche en fin de systole et en fin de diastole) chez le Dobermann après diagnostic échocardiographique de la maladie cardiaque (voir la rubrique « Mise en garde particulières »).
Contre-indications
Ne pas utiliser le pimobendane en cas de
cardiomyopathies hypertrophiques ou de maladies
pour lesquelles l’amélioration du débit cardiaque
n’est pas possible pour des raisons fonctionnelles ou
anatomiques (par exemple, une sténose aortique).
Ne pas utiliser en cas de dysfonctionnement hépatique
important car le pimobendane est principalement
métabolisé par le foie.
Ne pas utiliser en cas d’hypersensibilité à la substance
active ou à l’un des excipients.
Mises en garde particulières
Le médicament vétérinaire n’a pas été testé dans les cas de CMD asymptomatique chez les Dobermanns présentant une fibrillation atriale ou une tachycardie ventriculaire prolongée.
Précautions particulières pour une utilisation sûre chez
les espèces cibles :
Chez les chiens atteints de diabète sucré, la glycémie
doit être contrôlée régulièrement durant le traitement
avec le pimobendane.
Pour l’utilisation au « stade préclinique » de la
cardiomyopathie dilatée (asymptomatique avec
augmentation du diamètre ventriculaire gauche en
fin de systole et en fin de diastole), un diagnostic doit
être établi au moyen d’un examen cardiaque complet
(incluant un examen échocardiographique et, si
possible, un enregistrement Holter).
La surveillance de la fonction et de la morphologie cardiaques est recommandée chez les animaux traités avec le pimobendane.
Il est à noter pour les chiens allergiques aux protéines animales, que le produit est exempt de toute protéine animale.
Précautions particulières à prendre par la personne qui
administre le médicament vétérinaire aux animaux :
Les personnes présentant une hypersensibilité connue
au pimobendane ou à l’un des excipients doivent éviter
tout contact avec le médicament vétérinaire.
Ce médicament vétérinaire peut provoquer une
irritation de la peau et des yeux. Éviter tout contact
avec la peau et les yeux. En cas de contact avec les
yeux ou avec la peau, rincez-les immédiatement et
abondamment avec de l’eau. Se laver les mains après
utilisation.
Une ingestion accidentelle, notamment chez l’enfant,
peut entraîner l’apparition d’une tachycardie, d’une
hypotension orthostatique, de rougeurs au visage et de
maux de tête.
Pour éviter toute ingestion accidentelle, ne pas laisser la
seringue remplie sans surveillance et conserver le flacon
et la seringue en cours d’utilisation dans l’emballage
d’origine afin d’éviter que les enfants n’aient accès au
médicament vétérinaire.
Fermer hermétiquement et immédiatement le flacon
avec le bouchon après prélèvement de la quantité de
solution nécessaire.
Le médicament vétérinaire doit être utilisé et gardé hors
de la vue et de la portée des enfants.
En cas d’ingestion accidentelle, demandez
immédiatement conseil à un médecin et montrez-lui la
notice ou l’étiquette.
Gestation et lactation :
L’innocuité du médicament vétérinaire n’a pas été
établie chez les chiennes gestantes ou allaitantes.
L’utilisation ne doit se faire qu’après évaluation du
rapport bénéfice/risque établie par le vétérinaire
responsable.
Les études de laboratoire menées chez des rats et des
lapins n’ont pas mis en évidence d’effets tératogènes
ou foetotoxiques. Cependant, ces études ont mis en
évidence des effets maternotoxiques et embryotoxiques
à fortes doses, et ont aussi montré que le pimobendane
est excrété dans le lait.
Interactions médicamenteuses et autres formes
d’interactions :
Aucune interaction entre l’ouabaïne (strophantine),
glycoside cardiaque, et le pimobendane n’a été
observée dans les études pharmacologiques.
L’accroissement de la contractilité cardiaque induite
par le pimobendane est atténué par les inhibiteurs
calciques vérapamil et diltiazem et par le bêtabloquant
propranolol.
Surdosage :
Un surdosage peut provoquer un effet chronotrope
positif, des vomissements, une apathie, une ataxie,
des souffles cardiaques ou une hypotension. Il est
alors nécessaire de réduire la dose et d’instaurer un
traitement symptomatique approprié.
Lors d’une exposition prolongée (6 mois) chez le
chien Beagle sain de 3 à 5 fois la dose recommandée,
un épaississement de la valvule mitrale et une
hypertrophie ventriculaire gauche ont été observés
chez certains chiens. Ces changements sont d’origine
pharmacodynamique.
Incompatibilités majeures :
En l’absence d’études de compatibilité, ce médicament
vétérinaire ne doit pas être mélangé avec d’autres
médicaments vétérinaires.
Effets indésirables
Chiens :
Rare (1 à 10 animaux / 10 000 animaux traités) :
- Vomissements1, diarrhée2
- Anorexie2, léthargie2
- Augmentation du rythme cardiaque1,3
- Augmentation de la régurgitation mitrale4
Très rare (< 1 animal / 10 000 animaux traités,
y compris les cas isolés) :
- Pétéchies sur les muqueuses5, hémorragie (souscutanée)5
1. Ces effets sont dose-dépendants et peuvent être évités en réduisant la dose administrée.
2. Transitoire
3. Due à un léger effet chronotrope positif.
4. Observé durant le traitement de longue durée avec du pimobendane, chez des chiens souffrant de maladie valvulaire mitrale.
5. La relation de causalité avec le pimobendane n’a pas été clairement établie ; ces signes disparaissent à l’arrêt du traitement.
Il est important de notifier les effets indésirables. La
notification permet un suivi continu de l’innocuité d’un
médicament. Si vous constatez des effets indésirables,
même ceux ne figurant pas sur cette notice, ou si vous
pensez que le médicament n’a pas été efficace, veuillez
contacter en premier lieu votre vétérinaire.
Vous pouvez également notifier tout effet indésirable
au titulaire de l’autorisation de mise sur le marché ou
à son représentant local en utilisant les coordonnées
figurant à la fin de cette notice, ou par l’intermédiaire de
votre système national de notification :
FR : Agence Nationale du Médicament Vétérinaire (ANMV)
Site internet : https://pharmacovigilance-anmv.anses.fr/
BE : adversedrugreactions_vet@fagg-afmps.be
LU : luxvet@ms.etat.lu
Posologie pour chaque espèce, voies et mode d’administration
Voie orale.
Ne pas agiter le flacon avant ou pendant l’utilisation pour éviter la formation de mousse.
Afin de garantir une posologie appropriée, le poids
corporel doit être déterminé aussi précisément que
possible.
Respecter la fourchette de dose de 0,2 à 0,6 mg de
pimobendane/kg de poids corporel, divisée en deux
prises quotidiennes.
La dose quotidienne conseillée est de 0,5 mg de pimobendane/kg de poids corporel, divisée en deux prises quotidiennes espacées d’environ 12 heures (soit 0,25 mg/kg de poids corporel chacune équivalant à 0,17 ml du médicament vétérinaire 2 fois par jour).
La solution doit être prélevée à l’aide de la seringue
doseuse fournie dans l’emballage.
La seringue est graduée en kg de poids corporel avec
des graduations de 0,5 kg jusqu’à 12 kg et s’adapte
au flacon. Chaque graduation de 1 kg correspond à
0,25 mg de pimobendane.
Le poids total de l’animal doit être pris en compte pour
chaque administration. Par exemple, pour un chien de
6 kg, le médicament vétérinaire doit être prélevé jusqu’à
la graduation de 6 kg sur la seringue pour chaque
administration (cela équivaut à une dose de 0,25 mg de
pimobendane/kg de poids corporel par administration).
Ne pas dépasser la dose recommandée.
Chaque dose doit être administrée à jeun directement
dans la gueule de l’animal, environ une heure avant le
repas. Après administration, refermer soigneusement
le flacon à l’aide du bouchon. Après chaque utilisation,
nettoyez l’extérieur de la seringue en essuyant avec
un chiffon ou un mouchoir propre et sec. Le tissu
contaminé doit être immédiatement jeté.
Si la seringue se bouche, rincez-la à l’eau sans retirer
le piston et essuyez l’extérieur avec un chiffon ou un
mouchoir propre. Pour éviter toute contamination,
utilisez uniquement la seringue fournie pour
administrer cette solution buvable. La seringue utilisée
doit être conservée avec le médicament vétérinaire dans
l’emballage d’origine.
Le pimobendane peut être utilisé en association avec un diurétique, comme le furosémide par exemple.
Indications nécessaires à une administration correcte
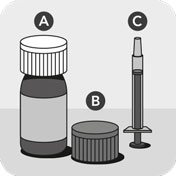
Le médicament vétérinaire se compose d’un flacon scellé par un bouchon avec sécurité enfant A, d’un second bouchon avec sécurité enfant avec un adaptateur intégré B et d’une seringue doseuse graduée en kg de poids corporel de type C.
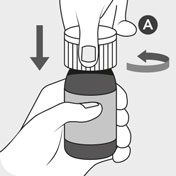
Ne pas agiter le flacon avant utilisation (ceci évite la formation de mousse). Ouvrir le flacon en position verticale en appuyant sur le bouchon de sécurité enfant A et en tournant simultanément le bouchon dans le sens inverse des aiguilles d’une montre. Jeter le bouchon blanc A.
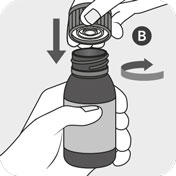
Fermer hermétiquement le flacon à l’aide du bouchon B et tourner simultanément le bouchon dans le sens des aiguilles d’une montre. Le bouchon B contient un adaptateur intégré qui doit se fixer automatiquement sur le flacon A. Vérifiez que le bouchon est bien fermé pour insérer correctement l’adaptateur.
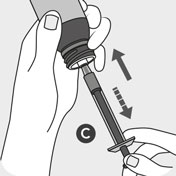
Retirez le bouchon B du flacon en appuyant sur le bouchon
de sécurité enfant et en tournant simultanément le bouchon
dans le sens inverse des aiguilles d’une montre et insérer
doucement l’extrémité de la seringue doseuse C sur
l’adaptateur du flacon.
Retournez le flacon et la seringue.
Tirez le piston et remplissez la seringue jusqu’à la dose
prescrite par votre vétérinaire.
Retourner le flacon en position verticale et retirer la seringue
doseuse du flacon.
Fermer le flacon avec le bouchon B.
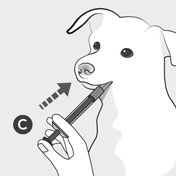
Placez l’extrémité de la seringue C dans la gueule de votre chien et poussez le piston pour administrer la dose prescrite.
L’information est également disponible en suivant ce lien : info.vetmedin.com/eu

Temps d’attente
Sans objet.
Précautions particulières de conservation
Tenir hors de la vue et de la portée des enfants.
À conserver en dessous de 30 °C.
Durée de conservation après première ouverture du
conditionnement primaire : 8 semaines.
Ne pas utiliser ce médicament vétérinaire après la date
de péremption figurant sur la boîte et le après Exp. La
date de péremption correspond au dernier jour du mois
indiqué.
Précautions particulières d’élimination
Ne pas jeter les médicaments dans les égouts ou dans
les ordures ménagères.
Utiliser des dispositifs de reprise mis en place pour
l’élimination de tout médicament vétérinaire non utilisé
ou des déchets qui en dérivent, conformément aux
exigences locales et à tout système national de collecte
applicable. Ces mesures devraient contribuer à protéger
l’environnement.
Demandez à votre vétérinaire ou à votre pharmacien
comment éliminer les médicaments dont vous n’avez
plus besoin.
Classification des médicaments vétérinaires
Médicament vétérinaire soumis à ordonnance.
Numéros d’autorisation de mise sur le marché et présentations
BE : BE-V664358
FR : FR/V/0375839 3/2025
LU : V 642/11/03/2025
Boîte en carton contenant 1 flacon rempli avec 50 ml et 1 seringue doseuse avec une échelle en kg de poids corporel, avec des graduations de 0,5 kg.
Date à laquelle la notice a été révisée pour la dernière fois
BE : 05/2025
FR : 04/2025
LU : 05/2025
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health. europa.eu/veterinary).
Coordonnées
Titulaire de l’autorisation de mise sur le marché et
fabricant responsable de la libération des lots :
Boehringer Ingelheim Vetmedica GmbH
55216 Ingelheim/Rhein, Germany
Représentant local et coordonnées pour notifier les
effets indésirables présumés :
France :
Boehringer Ingelheim Animal Health France SCS
29, avenue Tony Garnier
69007 Lyon, France
Tél : +33 4 72 72 30 00
Belgique/Luxembourg :
Boehringer Ingelheim Animal Health Belgium SA
Avenue Arnaud Fraiteurlaan 15-23
1050 Bruxelles, Belgique
+32-2-773.34.56
Autres informations
Vetmedin® est une marque déposée de Boehringer Ingelheim Vetmedica GmbH, utilisée sous licence.
